9月16日,阿斯利康宣布FDA授予Farxiga(达格列净)心衰适应症快速通道资格,用于降低射血分数减少(HFrEF)或射血分数保留(HFpEF)心衰患者的心血管死亡或心衰住院风险。
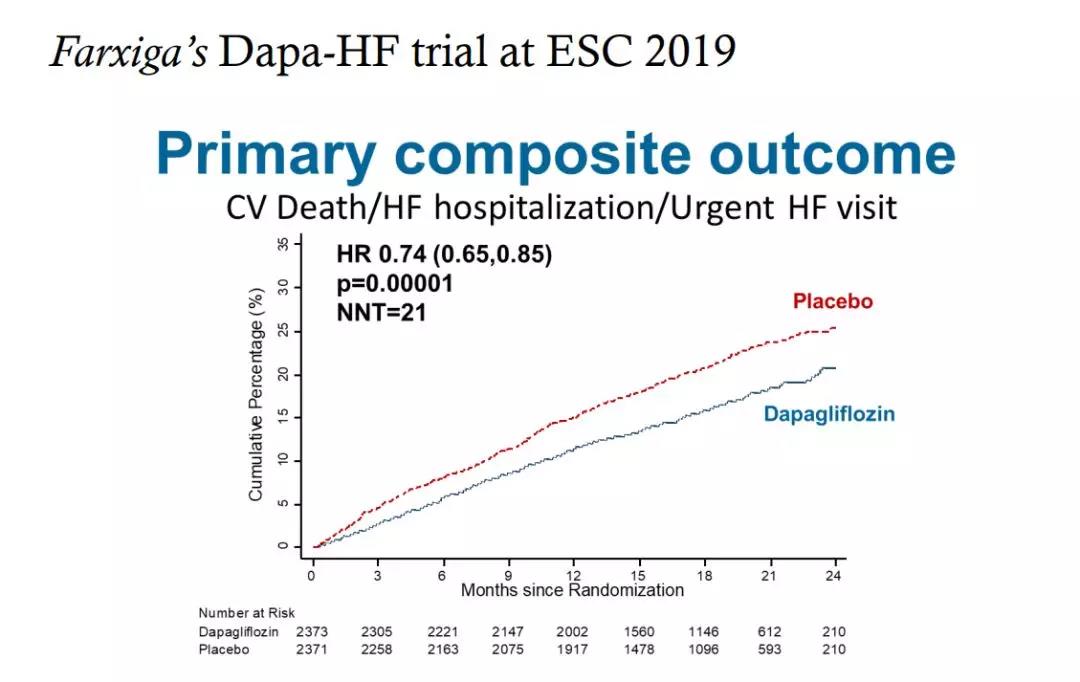
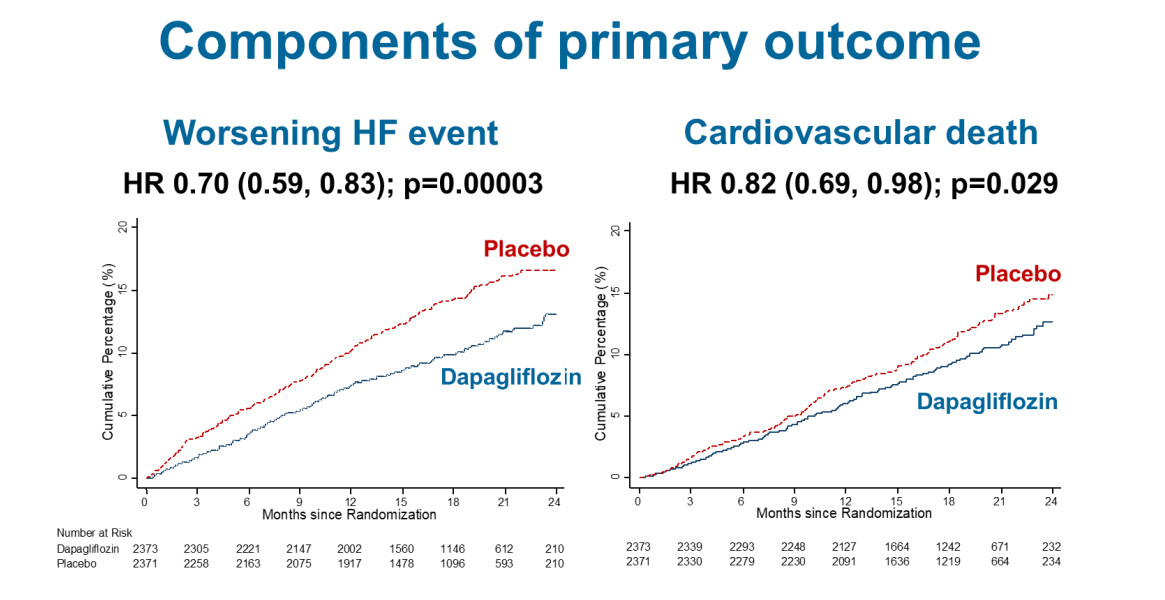
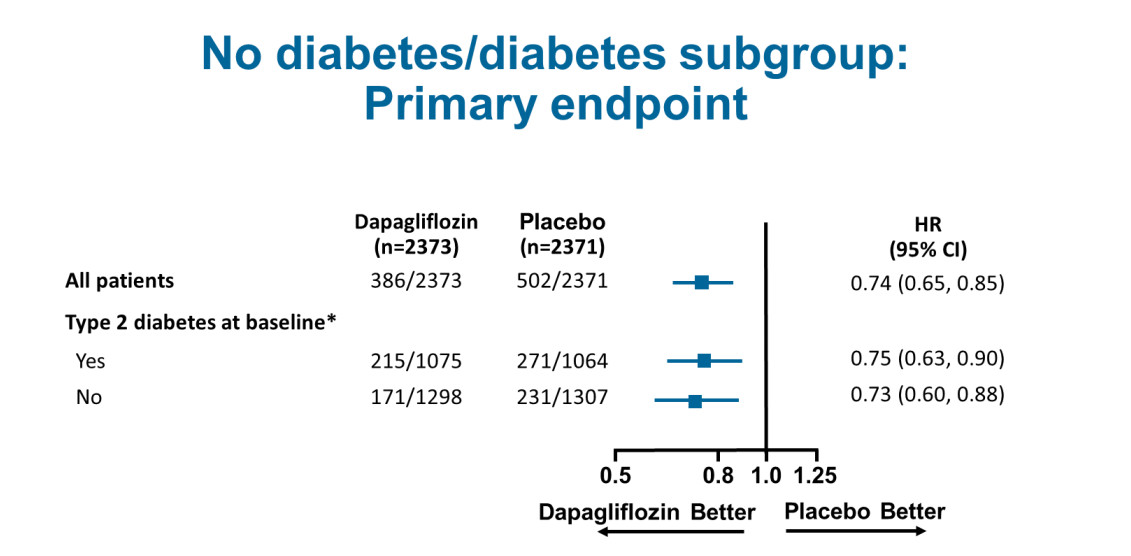
FDA此项授予主要依据III期DAPA-HF研究和DELIVER研究的结果,这两项研究分别考察了达格列净对HFrEF患者和HFpEF患者的疗效。8月20日,阿斯利康曾宣布DAPA-HF研究到达主要终点,达格列净成为首个被证实可以降低非2型糖尿病患者心血管死亡和心衰恶化风险的SGLT-2抑制剂。详细数据在9月初的ESC2019大会上公布,达格列净在标准治疗基础上能显著降低心血管(CV)死亡或心力衰竭恶化的主要复合终点发生风险26%。另外,达格列净组心力衰竭首次恶化的发生风险下降30%,因心血管疾病导致的死亡风险下降18%。
FDA的快速通道旨在加速一些针对临床需求未得到满足新药的开发和审评,企业可以在药物研发的任一阶段提出申请,FDA在60天内确认,确认后会给申请人提供更多沟通交流机会和指导,允许申请人滚动提交NDA和BLA上市申请资料,缩短这类新药的审评上市时间。8月27日,阿斯利康还曾宣布达格列净获得FDA授予的用于延缓肾功能衰竭进展并预防慢性肾病患者的心血管和肾脏死亡风险的快速通道资格。达格列净目前仅凭2型糖尿病的适应症已经是一个年销售额近14亿美元的重磅炸弹。今年3月25日被欧盟批准作为胰岛素的辅助疗法用于单用最优剂量胰岛素控制血糖不佳的1型糖尿病患者,是首个获批用于1型糖尿病的SGLT-2抑制剂。如今在不到一个月时间内接连获得两项FDA授出的快速通道资格,并且还是心衰、肾病大适应症。可以说,在通向“神药”的道路上,达格列净走出了自己飞一般的速度。
达格列净是一种钠-葡萄糖协同转运蛋白-2(SGLT-2)抑制剂。SGLT-2主要在肾脏表达,主要作用是帮助肾脏对葡萄糖的重吸收。SGLT-2抑制剂主要通过抑制SGLT-2的活动来减少肾脏对葡萄糖的重吸收,促进多余的葡萄糖通过尿液排出,进而发挥降糖作用。SGLT-2抑制剂是非胰岛素依赖性的降糖药,是糖尿病治疗的新途径。SGLT-2抑制剂这种降糖药用于治疗心衰的作用机制尚未完全阐明。截至目前,全球目前共批准上市了8款SGLT-2抑制剂类药物,其中托格列净、鲁格列净、伊格列净仅在日本获批。统计3个最受关注的SGLT-2抑制剂(默沙东埃格列净销售额未披露)可发现,SGLT-2抑制剂药物的市场规模在2018年已经超过40亿美元,2019年更是可能超过50亿美元。

市场份额方面,恩格列净虽然是第3家上市的SGLT-2抑制剂,但是借助EMPA-REG OUTCOME研究比卡格列净、达格列净提前2年获得了心血管获益的证据(具有较高风险心血管事件的2型糖尿病患者,在常规治疗基础上应用恩格列净治疗可使心血管死亡的相对风险降低38%,任何原因死亡的相对风险降低32%),并且在2016/12/2被FDA批准用于降低2型糖尿病患者心血管事件风险,所以目前暂居SGLT-2抑制剂市场的头牌,市场份额接近50%。达格列净凭借里程碑DECLARE研究也拿到了心血管获益的证据,虽然要到今年底之前才能在药品标签上添加“降低2型糖尿病患者心血管事件”的新适应症信息,但是在心衰适应症的开发速度上,达格列净遥遥领先竞品。阿斯利康最新半年财报显示,Farxiga将在2020H1向FDA提交心衰适应症的上市申请。恩格列净也正在进行针对心衰患者的大型III期EMPEROR项目,包括分别在射血分数降低心衰患者中进行的EMPEROR-Reduced研究,以及在射血分数保留的慢性心衰患者中进行的EMPEROR-Preserved 研究,主要评估恩格列净在降低心血管死亡和心衰住院方面的效果。EMPEROR项目合计入组超过8500例慢性心衰患者,以降低心血管死亡和心衰住院风险为主要终点,预计在2020年完成。
阿斯利康执行副总裁、生物制药研发负责人Mene Pangalos指出:“心衰影响全球大约6400万人,其中近一半会在确诊后5年内死亡。达格列净被FDA授予快速通道资格,将是我们实现预防、治疗甚至治愈心衰宏伟计划的关键一步。我们期待跟FDA密切沟通,将达格列净开发成为心衰患者的治疗新选择。”




