项目合作
PROJECT COOPERATION
【项目名称】????富马酸沃诺拉赞及片(Vonoprazanfumarate,TAK-438)????
【注册分类】化药3+3类
【商品名称】Takecab
【剂型规格】片剂5mg、10mg、20mg和40mg,其中20mg为推荐剂量。
【有效成分】Vonoprazan fumarate;TAK-438;化学名为1-[5-(2-Fluorophenyl)-1-(pyridine-3-ylsulfonyl)-1H-pyrrol-3-yl]-N-methylmethanaminefumarate(5-(2-氟苯基)-N-甲基-1-(3-吡啶基磺酰基)-1H-吡咯-3-甲胺富马酸盐);CAS号:1260141-27-2,881681-00-1(Vonoprazan),881681-01-2(Vonoprazan fumarate);它的分子式为C21H20FN3O6S,分子量为345.39,元素分析:C,54.66%;H,4.37%;N,9.11%;O, 20.80%;S,6.95%。化学结构式为:
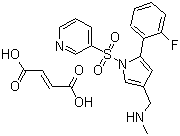
【国内外上市信息及适应症】
Takeda于2014年3月3日向日本厚生省提交新药申请(NDA),2014 年 12 月 26 日在日本获批上市,国内尚未上市。TAK-438用于胃食管反流(GERD),幽门螺杆菌感染,消化性溃疡,胃溃疡,十二指肠溃疡和食管炎等。
【药理药效】
富马酸沃诺拉赞属于可逆质子泵抑制剂,又称为钾离子竞争性酸阻滞剂,竞争性的阻断H+,K+-ATP酶(质子泵)K+结合位点,抑制了K+对H+,K+-ATP酶(质子泵)的结合作用,从而抑制了胃酸分泌。。
【用法用量及药代】
富马酸沃诺拉赞是继瑞伐拉赞(Revaprazan)后即将上市的第二个可逆质子泵抑制剂,瑞伐拉赞由Yuhan公司开发的可逆质子泵抑制剂,2007年获韩国FDA批准上市。与瑞伐拉赞相比,富马酸沃诺拉赞给药剂量低,瑞伐拉赞一天需口服药物100~200mg(规格100mg、200mg),而富马酸沃诺拉赞只需20mg。
【专利及行政保护情况】化合物专利:200680040789.7,申请日:2006年08月29日,到期日:2026年08月29日,法律状态:有权。工艺专利:201080018114.9,申请日:2010年02月24日,到期日:2030年02月24日,法律状态:审中-实审。组合物专利:WO2014003199,申请日:2013年6月26日,没有中文同族专利。
【产品优势】
(1) 与传统的不可逆质子泵抑制剂(如奥美拉唑、埃索美拉唑等)相比:
| 埃索美拉唑不足 | 沃诺拉赞优势 |
| PPI代谢的一种蛋白CYP2C19导致效果因人而异 | 竞争性抑制质子泵(即H+-K+-ATP酶)中的K+起作用,不主要经过由CYP2C19代谢 |
| 必须集中于胃壁细胞,经酸激活才可起作用 | 不需要集中于胃壁细胞及酸激活 |
| 持续时间14h,虽优于其他PPI类,但不能完全避免夜间酸突破现象 | 起效迅速,作用持久(24h) |
| 对酸不稳定,需做成肠溶剂型 | 对酸稳定,制成普通口服制剂即可 |
起效迅速,第1天给药就会达到最大的抑酸效果,且作用时间长;口服给药,不受胃酸破坏影响,毋需做成肠溶给药形式;对夜间酸突破现象有一定的改善作用。
(2)与同类可逆质子泵抑制剂瑞伐拉赞相比:
给药量少,降低不良反应。首次用药即可产生最大抑制效应,药效及起效剂量在不同患者中的差异不显著。
【市场前景】
消化性溃疡主要指发生于胃和十二指肠的慢性溃疡,是一多发病、常见病。溃疡的形成有各种因素,其中酸性胃液对粘膜的消化作用是溃疡形成的基本因素,因此得名。酸性胃液接触的任何部位,如食管下段、胃肠吻合术后吻合口、空肠以及具有异位胃粘膜的Meckel憩室。绝大多数的溃疡发生于十二指肠和胃,故又称胃、十二指肠溃疡。是卫生组织排名十大威胁人类生命安全的疾病之一。
现代生活节奏的加快,人们饮食规律不能保证,导致消化系统疾病发生率越来越高,其中胃肠病是最常见多发病,总发病率约占人口的20%左右。年龄越大,发生率越高,特别是50岁以上的中老年人更为多见,男性高于女性,如不及时治疗,长期发作极易转化成癌肿。胃肠病历来被医家视为疑难之证,一旦得病,应及时治疗、长期服药,才能控制或治愈。随着健康意识的不断普及,胃肠病用药市场需求将会越来越大。
2011年抗消化性溃疡及胃动力药物销售规模达到243.5亿美元,较2010年同期增长13.13%,持续着良好的增长势头。沃诺拉赞有望占据较大份额,市场前景良好。
【项目进度】
我公司工艺可以确保进行稳定的几十公斤以上级别的生产。
1、成本低,具有一定优势。
2、有关物质,产品稳定性做了较为详细的研究,符合SFDA原料药申报要求。
3、可以提供详细工艺路线及操作、分析方法、控制标准等相关资料
4、可根据需求交接工艺。
联系电话:0556-5032306
服务邮箱:service@bayeebio.com
